科学网—抑郁焦虑的共同神经环路
 精选
精选
已有 205 次阅读
2025-11-27 11:16
| 系统分类: 海外观察
动机缺失与威胁敏感性增强由相互重叠的脑区网络共同驱动
焦虑与抑郁被描述为人类面对共同痛苦源(如失去、痛苦或失败)时的两种不同反应。长期以来,精神病理学理论模型一直在推测这两种高发且共病的疾病之间的相互作用( 1),但关于二者共通神经环路的明确证据始终难以获取。在本期《科学》杂志,伍德(Wood)等人(2)报道了一组在狨猴中开展的精妙实验,揭示了大脑前额叶皮层中一套完整的神经环路——该环路可能在一定程度上是人类抑郁与焦虑两种行为特征的神经基础,这两种特征分别是:动机缺失(快感缺乏)与威胁敏感性增强。该研究还揭示了氯胺酮快速抗抑郁效应以及外侧前额叶皮层神经调节的潜在机制,这两种干预手段同样能缓解部分焦虑症状。综上,这些数据为理解焦虑与抑郁核心症状及其共病的神经底物提供了关键依据。
实验聚焦于此前被证实与抑郁及其治疗相关的多个前额叶脑区,包括背外侧前额叶皮层的布罗德曼 46区(dlPFC46)、胼胝体下扣带回皮层的25区(SCC25),以及前扣带回皮层的两个中间区域:32区(ACC32)和腹侧32区(ACC32v)(3, 4)。此前研究已证实,这三个脑区在解剖结构上相互连接,形成多突触通路——外侧前额叶区可通过该通路影响腹内侧皮层及皮层下区域的动机与情感加工过程。
伍德等人采用 “设计药物特异性激活设计受体”(DREADDs)技术,对狨猴的上述每个脑区进行依次失活。该方法的具体操作是:将含有编码设计型抑制性受体DNA的病毒载体注入目标脑区,随后通过让动物接触特定药物激活该受体,从而抑制该区域的神经活动。结果显示,失活投射至前扣带回皮层(ACC)的dlPFC46神经元后,狨猴为获取食物奖励而付出努力的意愿降低,且对感知到的威胁敏感性增强——这两种表现分别模拟了抑郁与焦虑的行为特征。此外,无论是通过全身注射,还是在SCC25局部注射临床有效剂量的氯胺酮进行预处理,均可阻断上述效应。此前针对狨猴(5)和人类(6)的研究表明,SCC25内部的过度激活可能与抑郁相关(3, 4)。伍德等人的研究在这些结果的基础上进一步证实,SCC25是介导氯胺酮快速抗抑郁效应的关键脑区。此外,作者还发现,失活dlPFC46-ACC投射对动机与威胁敏感性的影响,依赖于dlPFC46通过ACC32不同亚区与SCC25形成的间接连接:通过DREADDs特异性失活dlPFC46-ACC32投射会降低动机,但不影响威胁敏感性;而失活dlPFC46-ACC32v投射则会增强威胁敏感性,但不改变动机。由此,作者揭示了这两种行为背后既共通又独特的神经环路(见图)。
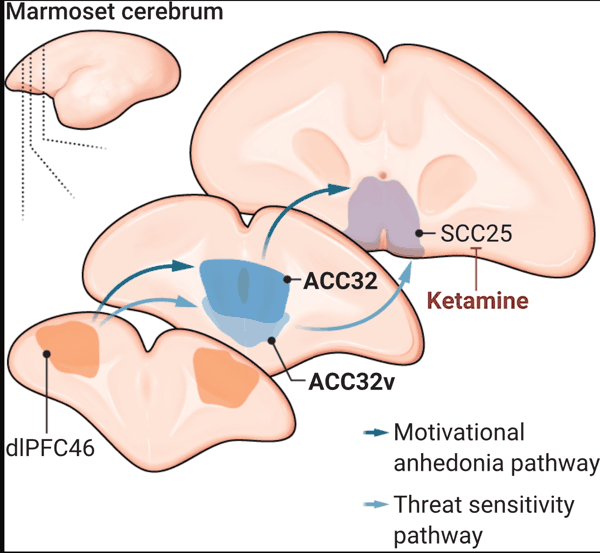
两条通路,两种症状
失活狨猴背外侧前额叶 46区(dlPFC46)向前扣带回皮层(ACC)的投射后,其为获取奖励而付出努力的意愿降低(动机性快感缺乏),且对入侵者的反应性增强(威胁敏感性)。而向胼胝体下扣带回皮层25区(SCC25)递送氯胺酮可阻断上述效应。dlPFC46对动机的影响依赖于其通过前扣带回32区(ACC32)与SCC25形成的连接,而对威胁敏感性的影响则依赖于其通过前扣带回腹侧32区(ACC32v)与SCC25形成的连接。
图示: A. 马斯汀(A. Mastin)/《科学》**
伍德等人的研究结果对理解抑郁与焦虑的生物学基础及其治疗具有多重重要意义。作者证实,尽管失活 dlPFC46-ACC32投射会显著降低狨猴为获取食物奖励而付出努力的意愿(即对奖励的“渴望”),但这种效应难以用以下因素解释:对食物的动机改变(无努力要求时)、运动功能受损,或对任务的认知理解障碍。作者还通过蔗糖偏好实验评估了上述脑区失活是否会改变动物对愉悦刺激的反应(享乐反应,即对奖励的“喜爱”),结果发现无显著影响。长期以来,在皮层下多巴胺信号(7, 8)及SCC25活动(5)的研究中,研究者已观察到动机反应与享乐反应的分离,但背外侧与内侧前额叶皮层环路在其中的作用仍不明确。
另一个值得关注的发现是, dlPFC46同时影响动机与威胁敏感性。为何背外侧前额叶皮层的同一区域会成为两种看似不同行为的神经基础?在灵长类动物中,背外侧前额叶皮层(dlPFC)主要与认知操作相关,如工作记忆、抽象推理和认知控制。一种可能的解释是:动物需要借助dlPFC的功能来克服肌肉疲劳与不适等外周信号,从而为获取食物付出努力(9)。类似的认知控制机制也可解释观察到的威胁反应增强——dlPFC46功能缺失会导致大脑过滤皮层下结构传来的威胁信号的能力下降。在人类中,对dlPFC进行非侵入性刺激会改变其他脑区(如双侧杏仁核)的威胁加工过程(10)。要验证这些可能性,还需开展进一步研究。
深入解析 “渴望”“喜爱”与威胁敏感性背后的神经通路,对精神疾病病理生理学的概念构建与评估具有关键意义。例如,目前针对重度抑郁中“快感缺乏”的标准诊断与临床评估,仍采用过于宽泛的定义(“兴趣或愉悦感丧失”),将“渴望”与“喜爱”的障碍视为可互换的症状(11)。这种情况也体现在新潜在治疗手段的临床试验行为评估中——这些评估往往无法区分动机改变与愉悦感改变(12)。此外,当前诊断标准也未考虑“抑郁患者的选择性动机缺失是否与共病性威胁敏感性存在特异性关联”这一问题。相比之下,伍德等人的研究提示:同时存在选择性动机缺失与威胁反应增强的患者,可能会从针对dlPFC的治疗中获益,如经颅磁刺激(TMS)(13)。相反,若患者仅表现出低动机而无焦虑症状,其背后的机制可能不涉及dlPFC,例如炎症抑制多巴胺释放(12)或SCC25直接功能异常(4)。这类患者可能更适合抗炎治疗、促多巴胺能干预,或针对SCC25的治疗(如深部脑刺激,甚至可能是氯胺酮)。最后,对于以“愉悦感丧失”为主要症状、但动机无真正改变的患者,可能需要一套完全不同的干预方案(11)。
下一步的关键研究方向是:明确人类大脑中是否存在类似的平行环路功能。如今,随着低频率聚焦超声( 14)、时间干扰刺激(15)等非侵入性深部脑刺激技术的发展,这一目标已具备实现的可能——这些技术可让研究者在不干扰中间脑组织的前提下,对大脑深部结构的活动模式进行局部调节。尽管如此,伍德等人的研究仍标志着精神科精准医学研究迈出了重要一步。
转载本文请联系原作者获取授权,同时请注明本文来自孙学军科学网博客。 链接地址: https://blog.sciencenet.cn/blog-41174-1498891.html
上一篇: 2型糖尿病电场磁场治疗实验【2020】 下一篇: 体内电解槽植入释放氢气治疗疾病的创新概念
