科学网—线粒体加持免疫细胞抗癌
 精选
精选
已有 217 次阅读
2026-4-4 08:34
| 系统分类: 博客资讯
线粒体加持免疫细胞抗癌
树突状细胞是固有免疫细胞,可调控抗肿瘤免疫应答的强度、幅度与持续时长。经典 1型树突状细胞(cDC1)在此过程中至关重要,但矛盾的是,其在大多数实体肿瘤中数量稀少且功能受损,这已成为免疫治疗起效的一大瓶颈。目前,肿瘤微环境中cDC1功能异常的分子机制尚不明确。本期第55页,游等人[1]报道: 线粒体健康状态是维持 cDC1功能的关键;同时在小鼠模型中证实,可通过干预恢复肿瘤微环境内的cDC1功能,为借助代谢重编程重塑树突状细胞、重建抗肿瘤免疫提供了理论框架。
肿瘤免疫的完整流程包括:固有免疫细胞识别肿瘤、肿瘤引流淋巴结内启动肿瘤特异性 T细胞、效应T细胞浸润至肿瘤组织,并在肿瘤微环境中持续发挥作用。树突状细胞可摄取、加工并呈递抗原,启动适应性免疫,全程参与上述抗肿瘤应答环节[2]。树突状细胞主要分为四类:经典1型(cDC1)、经典2型(cDC2)、浆细胞样、单核细胞来源型。其中cDC1专门负责向CD8⁺效应T细胞呈递肿瘤抗原。肿瘤内cDC1数量匮乏,主要归因于恶劣肿瘤微环境导致其迁移受阻、分化异常、存活能力下降[3-5]。除数量减少外,肿瘤微环境还会通过尚未阐明的机制,削弱残存cDC1的生理功能。
两类 cDC1细胞的差异机制
高线粒体膜电位 /线粒体探针比值(TMRM/MG高)的cDC1:线粒体功能健康,转录因子NRF1与线粒体蛋白OPA1协同促进氧化磷酸化;优异的线粒体功能可保障抗原呈递效率,增强CD8⁺T细胞的抗肿瘤活性。
反之,低比值( TMRM/MG低)的cDC1:线粒体外膜DRP1蛋白相对OPA1占比过高,引发线粒体碎片化,抑制OPA1-NRF1信号通路;ATP生成不足会激活AMPK依赖性自噬,导致I类主要组织相容性复合体(MHC-I)降解、抗原呈递受损,最终使CD8⁺T细胞抗肿瘤应答乏力。
线粒体依靠氧化磷酸化生成细胞核心能量物质三磷酸腺苷( ATP),该过程依赖稳定的线粒体膜电位。相较于cDC2,cDC1的线粒体总量、膜电位及氧化磷酸化水平均更高[6-7],但此前学界并不清楚线粒体功能如何调控cDC1介导的免疫应答。
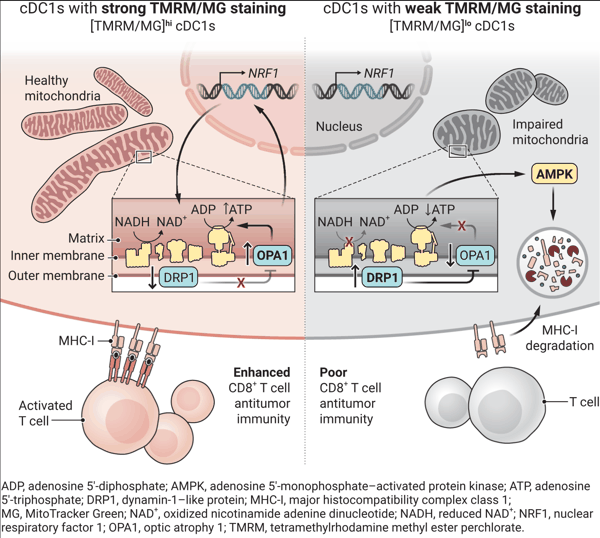
游团队利用四甲基罗丹明甲酯( TMRM)与线粒体绿色荧光探针(MG)两种染料,在小鼠体内鉴定出两类代谢特征截然不同的cDC1亚群:
1. TMRM/MG高亚群:线粒体膜电位高、氧化磷酸化能力强;
2. TMRM/MG低亚群:线粒体膜电位去极化、氧化磷酸化能力弱。
其中高比值亚群的细胞膜表面抗原呈递分子( MHC)表达更高,抗原呈递与T细胞激活能力显著优于低比值亚群。研究在小鼠正常组织及黑色素瘤、乳腺癌、肝癌等多种肿瘤中,均发现了TMRM/MG高cDC1;但随着肿瘤进展,该亚群占比与整体线粒体健康水平(膜电位)持续下降,证实线粒体稳态直接影响cDC1介导的抗肿瘤免疫。
游团队进一步证实,线粒体融合蛋白 OPA1是决定高比值cDC1特征的核心因子。OPA1参与线粒体内膜融合,可提升线粒体呼吸活性[8]。特异性敲除树突状细胞的OPA1基因,不会改变肿瘤内cDC1总数量,但会使其线粒体趋向去极化、高比值功能亚群减少,最终破坏适应性抗肿瘤免疫。
OPA1缺失会下调转录因子NRF1的活性;敲除NRF1可复刻OPA1缺失引发的cDC1功能缺陷,而过表达NRF1则能部分逆转损伤。NRF1可调控线粒体呼吸链复合体编码基因;在小鼠体内通过药物或基因手段抑制呼吸链复合体,会直接削弱cDC1激活T细胞的能力。这明确证明:完整的线粒体呼吸功能,是cDC1发挥抗肿瘤免疫的必要条件,也与既往研究中NRF1调控人类树突状细胞线粒体新生、参与细胞分化的结论相符[9]。
实验同时发现:敲除 cDC1的OPA1,不会影响细胞摄取抗原、迁移至肿瘤引流淋巴结,也不干扰初期T细胞激活;但会显著降低肿瘤内CD8⁺T细胞的丰度与抗肿瘤功能,说明OPA1主要负责维持肿瘤微环境内cDC1对T细胞的持续激活作用。
机制层面: OPA1不足会降低ATP合成,激活AMPK通路,诱发自噬介导的MHC-I蛋白降解,导致cDC1抗原呈递能力下降;通过药物或基因抑制自噬,可恢复细胞膜表面MHC-I水平。该研究首次建立了 线粒体健康 →能量代谢→抗原呈递 的明确通路,也印证了既往线粒体调控因子参与树突状细胞 MHC表达的相关结论[10-11]。
敲除 OPA1还会加剧线粒体碎片化、破坏内膜结构,与其线粒体融合的核心功能一致。关键验证实验显示:敲除DRP1(线粒体分裂关键蛋白)抑制线粒体分裂,可显著挽救OPA1缺失造成的cDC1功能障碍,证明线粒体融合-分裂的动态平衡,是保障cDC1活性的核心。
动物治疗实验显示:向小鼠肿瘤内注射 TMRM/MG高的功能性cDC1,可触发强效抗肿瘤免疫;联合免疫检查点抑制剂(激活抗肿瘤T细胞)可进一步放大疗效。临床研究早已证实,肿瘤内cDC1丰度与免疫检查点药物疗效正相关[12];而本研究进一步锁定**线粒体健康状态**是决定治疗响应的关键靶点,为开发树突状细胞靶向疗法开辟了新方向。
目前该调控机制是否适用于其他抗原呈递细胞仍不明确;且该通路不存在于 cDC2中,说明不同树突状细胞亚群拥有专属的代谢调控网络。肿瘤演进过程中,缺氧、营养竞争、慢性炎症、代谢副产物等肿瘤微环境信号,究竟何种因素诱发cDC1线粒体去极化,仍有待后续深入探究。
转载本文请联系原作者获取授权,同时请注明本文来自孙学军科学网博客。 链接地址: https://blog.sciencenet.cn/blog-41174-1528637.html
上一篇: 衰老细胞的代谢特征类似肿瘤细胞 下一篇: 为何部分抗癌免疫细胞会在肿瘤内部丧失战斗力
